医疗卫生:第二批中国药品监管科学行动计划重点项目已启动
文/剑鱼标讯
2022-12-05
 1
1
文章摘要:11月21日,国家药品监督管理局医疗器械技术审评中心发布《关于第二批中国药品监管科学行动计划重点项目《生物3D打印新材料及产品性能评价技术研究》信息征集的通知 》(以下简称“通知”)。
11月21日,国家药品监督管理局医疗器械技术审评中心发布《关于第二批中国药品监管科学行动计划重点项目《生物3D打印新材料及产品性能评价技术研究》信息征集的通知 》(以下简称“通知”)。原文如下:
关于第二批中国药品监管科学行动计划重点项目《生物3D打印新材料及产品性能评价技术研究》信息征集的通知
各有关单位:
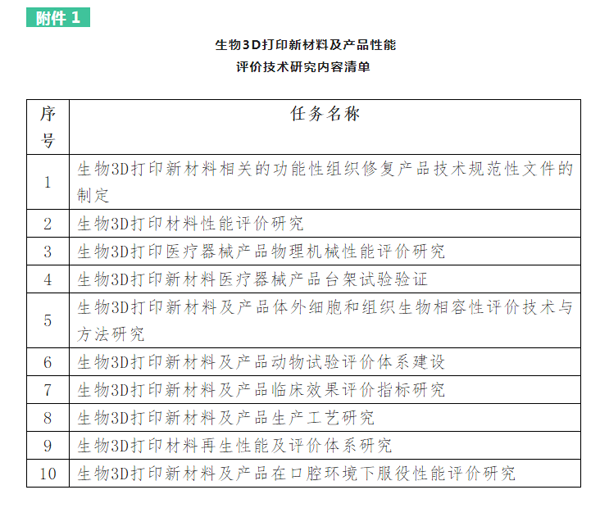
根据国家药监局《关于实施中国药品监管科学行动计划第二批重点项目的通知》(国药监科外〔2021〕37号)的要求,我中心承担并开展生物3D打印新材料及产品性能评价技术研究工作。该项目依托国家药监局监管科学研究基地和重点实验室,联合国内重点高校、科研院所、临床机构等,针对健康医疗和产业发展亟需的生物3D打印新材料、新技术、新原理等创新型医疗器械开展了相关研究工作,研究内容清单详见附件1。
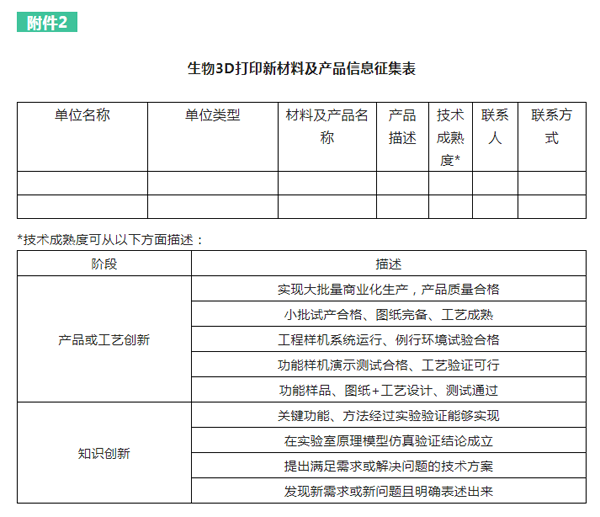
根据项目研究工作需要,现面向社会公开征集关于生物陶瓷、陶瓷/PEEK复合材料、生物活性骨修复材料、口腔可吸收修复膜材料及整形材料等五类生物3D打印组织修复医疗器械的研发和生产信息。邀请具有相关研发基础的境内外生产企业、科研院所、临床机构等积极参与。
请有意向参与的单位填写信息征集表(详见附件2),并于2022年12月16日前以电子邮件形式报送我中心,邮件主题及文件名称以“第二批监管科学+生物3D打印+企业名称”进行命名。
联系人:阿茹罕、吴静、金乐
电话:010-86452824、010-86452807、010-86452802
电子邮箱:ahr@cmde.org.cn、wujing@cmde.org.cn、jinle@cmde.org.cn
关于械企服
械企服隶属于著名招投标大数据服务平台剑鱼标讯,为旗下医械通产品专属公众号。
医械通是专为医械企业量身定制的数字化服务平台,拥有专业的数据采集解析、整合处理能力,基于医械市场5大数据库可实现各类医械产业上下游数据精准覆盖。

 1
1